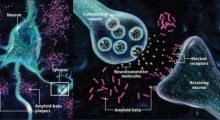
Alzheimer, Parkinson e Corea di Huntington sono tre malattie con una cosa in comune: sono causate da proteine mal ripiegate che formano grumi insolubili nel cervello dei pazienti affetti e, infine, ne distruggono le cellule nervose.
Una delle questioni più importanti nel campo delle scienze biologiche e della medicina è perciò: come fanno le proteine - gli strumenti delle cellule viventi - a raggiungere o a perdere la loro struttura tridimensionale. Perché possono svolgere i loro compiti in modo corretto solo se le loro catene di aminoacidi sono ben ripiegate.
Ma finora è stato quasi impossibile indagare su cosa succede esattamente quando le proteine si piegano o si aprono. Con il calore e la pressione, le proteine perdono facilmente la loro forma - e quindi la loro funzione. Tuttavia, questi metodi non sono adatti per osservare direttamente il loro processo di dispiegamento. Le forme intermedie che si formano nel corso del ripiegamento delle proteine sono troppo transitorie.
Per la prima volta e con un approccio innvativo, dei ricercatori sono riusciti a "filmare" il complesso processo di folding [piegatura] delle proteine. Gli scienziati del Max Planck Institute for Biophysical Chemistry (MPIbpc) e del Centro tedesco per le Malattie Neurodegenerative (DZNE) di Göttingen, insieme ai colleghi dell'Accademia Polacca delle Scienze di Varsavia e dell'Università di Varsavia, hanno reso visibile - a risoluzione atomica - come una proteina "perde la sua forma" progressivamente.
Per farlo, i ricercatori avevano riposto le speranze sulle basse temperature. "Se una proteina viene raffreddata lentamente, le sue forme intermedie sono molte di più rispetto ai metodi di denaturazione comunemente usati, come il calore, la pressione, o l'urea. Speravamo che tali varianti sarebbero state sufficienti per esaminare le forme intermedie con la risonanza magnetica nucleare (NMR)", scrive Markus Zweckstetter, responsabile dei gruppi di ricerca "Determinazione della struttura proteica con MNR" al MPIbpc e "Biologia Strutturale nella Demenza" al DZNE di Göttingen.
Come una proteina perde la sua forma
Come oggetto della ricerca, il team di Zweckstetter ha scelto una proteina chiave per la produzione di tossine nell'Enterococcus faecalis, un agente patogeno frequente negli ospedali dove rischia in particolare di comprometterei i pazienti con un sistema immunitario debole. Ma questa non è l'unica ragione per cui la cosiddetta proteina CylR2 è interessante.
Qualche tempo fa, i ricercatori che lavorano con Stefan Becker al MPIbpc sono riusciti a chiarire la sua struttura, che mostra una forma tridimensionale; ciò rende la CylR2 un candidato particolarmente promettente per l'approccio degli scienziati. "La ClyR2 è una proteina relativamente piccola composta da due subunità identiche. Questo ci ha dato la grande opportunità di visualizzare le singole fasi del suo processo di dispiegamento in provetta", spiegano i chimici Mariusz e Lukasz Jaremko.
Il gruppo di Stefan Becker ha intrapreso il primo passo: preparare una quantità sufficiente della proteina in laboratorio. Successivamente, i due chimici hanno raffreddato la proteina da 25°C a -16°C ed hanno esaminato le sue forme intermedie con la spettroscopia NMR. Hanno raggiunto ciò che speravano: il loro "filmato" mostra a risoluzione atomica come si dispiega la proteinaa poco a poco.
Il biologo strutturale Markus Zweckstetter descrive esattamente ciò che accade in questo processo: "Vediamo chiaramente come la proteina CylR2, in ultima analisi, si divide nelle sue due subunità. Le singole subunità sono inizialmente relativamente stabili. Dopo un ulteriore raffreddamento, la proteina continua ad aprirsi e a -16°C è estremamente instabile e dinamica. Questa forma instabile della proteina fornisce il seme per la piegatura e può anche essere l' "innesco" del misfolding [=errata piegatura]".
I risultati dello scienziato possono aiutare a raggiungere una maggiore comprensione di come le proteine assumono la loro struttura spaziale e perché le forme intermedie di alcune proteine si piegano erroneamente nel caso di malattia.
![]() Read the original English version of this article here.
Read the original English version of this article here.
***********************
Cosa pensi di questo articolo? Ti è stato utile? Hai rilievi, riserve, integrazioni? Conosci casi o ti è successo qualcosa che lo conferma? o lo smentisce? Puoi usare il modulo dei commenti qui sotto per dire la tua opinione. Che è importante e unica.
***********************
Fonte: Materiale del Max Planck Institute for Biophysical Chemistry.
Riferimento:Mariusz Jaremko, Łukasz Jaremko, Hai-Young Kim, Min-Kyu Cho, Charles D Schwieters, Karin Giller, Stefan Becker, Markus Zweckstetter. Cold denaturation of a protein dimer monitored at atomic resolution. Nature Chemical Biology, 2013; DOI: 10.1038/nchembio.1181.
Pubblicato in Science Daily il 11 Febbraio 2013 - Traduzione di Franco Pellizzari.
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari proposti da Google sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.
| Sostieni l'Associazione; una donazione, anche minima, ci aiuterà ad assistere malati e famiglie e continuare ad informarti. Clicca qui a destra: |






 Associazione Alzheimer OdV
Associazione Alzheimer OdV