 Neuroni con microscopio ZEISS.
Neuroni con microscopio ZEISS.
Alti livelli di calcio sono tossici per le cellule e contribuiscono alla perdita di neuroni nel morbo di Alzheimer (MA). Un nuovo studio su JCI Insight ha identificato un meccanismo attraverso il quale il cervello giovane si protegge da alti livelli di calcio e potrebbe aiutare gli scienziati a imparare come proteggere il cervello da questa devastante condizione neurodegenerativa.
La gliossalasi 1 (GLO1) è una proteina con un ruolo essenziale per eliminare i sottoprodotti tossici delle cellule. Nello studio, i ricercatori della Yale University di New Haven (Connecticut/USA) hanno scoperto livelli elevati di GLO1 nel cervello di animali con livelli eccessivi di calcio cellulare, scoprendo che il cervello aumenta l’espressione di GLO1 come meccanismo protettivo per mitigare gli effetti della disregolazione del calcio.
Tuttavia, con l’avanzare dell’età, l’attività della GLO1 diminuisce, il che potrebbe rendere il cervello meno resistente alla neurodegenerazione. Lo studio, una collaborazione tra i laboratori di Amy Arnsten PhD, prof.ssa di neuroscienze, e di Lauren Hachmann Sansing MD, professore di neurologia della Yale, potrebbe favorire lo sviluppo di terapie che puntano la GLO1 per prevenire la neurodegenerazione. "Abbiamo scoperto che il cervello stesso affronta la perdita di calcio e usa un fattore di resilienza che si erode con l'età", afferma Amy Arnsten, coautrice senior dello studio. “Se potessimo mantenere attivo questo meccanismo, proteggeremmo il cervello in un modo ideato dal cervello stesso”.
Come la disregolazione del calcio influisce sul cervello
Il laboratorio della Arnsten si concentra sulla disregolazione del calcio in un canale noto come 'recettore 2 della rianodina' (RyR2), che rilascia il calcio dal deposito all’interno del reticolo endoplasmatico liscio di una cellula. "Questo canale è come un rubinetto che puoi aprire e chiudere", afferma Elizabeth Woo, dottoranda di Yale e prima autrice dello studio. "Può far sì che il calcio fuoriesca nel neurone, il che ha molti effetti a valle". Precedenti ricerche hanno dimostrato che l'RyR2 può alterarsi con l’età in modo che il rubinetto sia costantemente 'aperto' e che questi cambiamenti sono associati al MA e persino al Long COVID.
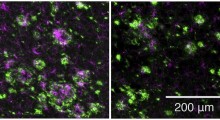
Nel nuovo studio, i ricercatori hanno esplorato come il cervello risponde a questo afflusso non regolato di calcio. Il team ha usato un modello animale in cui l'RyR2 è stato geneticamente modificato per essere sempre 'attivo', causando una perdita cronica di calcio nel cervello. Hanno osservato un’elevata espressione e attività di GLO1 sia nella corteccia prefrontale che nell’ippocampo, due regioni importanti per la cognizione e la memoria. L’espressione di GLO1 inizialmente aumentava con l’età, raggiungendo il picco a 12 mesi nei topi, ma poi diminuiva negli animali più anziani.
Quindi, i ricercatori hanno messo gli animali più anziani in un labirinto a forma di T progettato per testare la loro memoria. Hanno scoperto che quelli con recettori RyR2 geneticamente modificati, con poca GLO1, avevano una memoria peggiore rispetto alle loro controparti sane. I risultati hanno confermato che la disfunzione del calcio è associata a un peggioramento della cognizione. Lo studio indica l’espressione di GLO1 come un potenziale meccanismo nel cervello per compensare la disregolazione cronica del calcio. "Il calcio è un mediatore molto potente nel cervello", afferma la Woo. "La GLO1 ha proprietà disintossicanti che possono aiutare il cervello a contrastare i cambiamenti del calcio nel tempo".
I ricercatori sperano che la scoperta dei processi che precedono il MA possa un giorno portare a nuove terapie. "Ci sono molte importanti ricerche parallele che esaminano come trattare il MA una volta che si è sviluppato", dice la Woo. “Ma man mano che la biologia a monte diventa più chiara, possiamo anche sviluppare terapie preventive per colpire la malattia prima che diventi un problema”.
Fonte: Yale University (> English) - Traduzione di Franco Pellizzari.
Riferimenti: E Woo, [+21], LH Sansing. Ryanodine receptor 2–mediated calcium leak is associated with increased glyoxalase I in the aging brain. JCI Insight, 2025, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.






 Associazione Alzheimer OdV
Associazione Alzheimer OdV