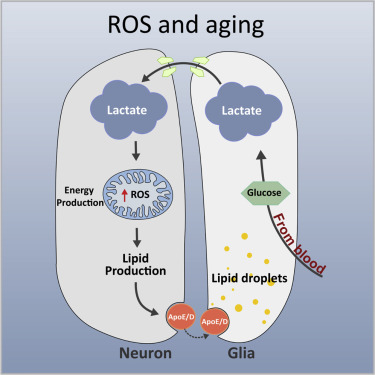
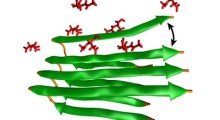
 La fruttuosa collaborazione metabolica tra neurone e cellula glia, che viene interrotta dall'eccesso di radicali liberi, dando inizio alla neurodegenerazione. (Fonte: Liu et al.)Dei ricercatori hanno scoperto che compromettere una collaborazione cruciale tra le cellule del cervello può portare alla neurodegenerazione.
La fruttuosa collaborazione metabolica tra neurone e cellula glia, che viene interrotta dall'eccesso di radicali liberi, dando inizio alla neurodegenerazione. (Fonte: Liu et al.)Dei ricercatori hanno scoperto che compromettere una collaborazione cruciale tra le cellule del cervello può portare alla neurodegenerazione.
Lo studio, pubblicato su Cell Metabolism, riferisce di un meccanismo attraverso il quale due tipi di cellule cerebrali, neuroni e glia, di norma supportano le rispettive funzioni.
I ricercatori hanno scoperto che, quando questo meccanismo si interrompe, nasce una neurodegenerazione, aprendo la strada a una migliore comprensione di disturbi come l'Alzheimer.
L'autore senior dottor Hugo J. Bellen, professore di neuroscienze e genetica molecolare e umana al Baylor College of Medicine e ricercatore dell'Howard Hughes Medical Institute, ha dichiarato:
"Usando moscerini della frutta, possiamo studiare approfonditamente le funzioni delle proteine che sono condivise tra questi insetti e gli esseri umani.
"Spesso, la perturbazione di queste proteine porta a caratteristiche neurodegenerative nei moscerini e alle malattie neurodegenerative delle persone. Studiando il modo in cui questi geni causano difetti nei modelli di moscerini e topi, possiamo migliorare le nostre conoscenze nei meccanismi connessi alla malattia umana".
La prima autrice Dott.ssa Lucy Liu PhD, neuroscienziata dal laboratorio di Bellen, ha scoperto nel 2015 che un certo numero di geni coinvolti nella neurodegenerazione promuovono i danni ai neuroni e alle glia inducendo livelli elevati di radicali liberi (stress ossidativo) e l'accumulo di gocce lipidiche nelle glia. Questo lavoro è stato la premessa per lo studio attuale. Spiega la Liu:
"Usando la microscopia elettronica, abbiamo osservato l'accumulo di gocce di lipidi nelle glia prima di ovvi sintomi di neurodegenerazione. In presenza di elevati livelli di stress ossidativo, i neuroni producono una sovrabbondanza di lipidi. La combinazione di radicali liberi e lipidi, che produce lipidi perossidati, è dannosa per la salute cellulare.
"I neuroni cercano di evitare questo danno mediante la secrezione di questi lipidi, e le apolipoproteine - le proteine che trasportano i lipidi - li trasportano alle cellule glia. Le glia conservano i lipidi in gocce, le separano dall'ambiente e provvedono al meccanismo di protezione".
La Liu e i suoi colleghi hanno scoperto che l'immagazzinamento delle goccioline lipidiche nelle glia protegge i neuroni dai danni, finché i radicali liberi non distruggono le goccioline lipidiche. Quando le gocce di lipidi sono distrutte, si verificano i danni cellulari e inizia la neurodegenerazione.
Collegamento con l'Alzheimer
La Liu ha scritto:
"La nostra ricerca ci ha portato ad un risultato affascinante e inatteso. Circa il 15% della popolazione umana è portatore dell'apolipoproteina APOE4. Dal momento che l'APOE4 è stato collegato per la prima volta all'Alzheimer quasi 30 anni fa, rimane il fattore di rischio genetico più conosciuto di questa malattia.
"Nel frattempo, l'APOE2, che è leggermente diverso dall'APOE4, è protettivo contro la malattia. Questa evidenza suggerisce che l'APOE è importante per una corretta funzione cerebrale, ma sappiamo poco su come l'APOE stesso porta all'Alzheimer".
I ricercatori hanno scoperto che le apolipoproteine APOE2, APOE3 e APOE4 hanno diverse abilità nel trasferire i lipidi dai neuroni alle glia e quindi differiscono nella loro capacità di mediare l'accumulo di gocce lipidiche. Dice la Liu:
"APOE2 e APOE3 possono trasferire efficacemente i lipidi nelle glia. Dall'altra parte, l'APOE4 è in pratica incapace di eseguire questo processo. Ciò comporta una mancanza di accumulo di gocce di lipidi nelle glia e il guasto del meccanismo di protezione che separa i lipidi perossidati. Questa differenza fondamentale nella funzione dell'APOE4 probabilmente prepara un individuo ad essere più suscettibile agli effetti dannosi dello stress ossidativo, che diventa elevato con l'età".
E Bellen commenta:
"Un altro contributo di questo studio è che le glia hanno un ruolo importante di protezione contro lo stress ossidativo nella neurodegenerazione. Le mutazioni che portano ad un guasto di questo sistema di sostegno tra i neuroni e la glia possono aprire la strada alla neurodegenerazione e sembra che i radicali liberi siano alla base di un aspetto chiave di questo processo".
Fonte: Baylor College of Medicine® (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Lucy Liu, Kevin R. MacKenzie, Nagireddy Putluri, Mirjana Maletić-Savatić, Hugo J. Bellen.The Glia-Neuron Lactate Shuttle and Elevated ROS Promote Lipid Synthesis in Neurons and Lipid Droplet Accumulation in Glia via APOE/D. Cell Metabolism, Published: September 28, 2017. DOI: 10.1016/j.cmet.2017.08.024
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali colelgamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.







 Associazione Alzheimer OdV
Associazione Alzheimer OdV