A volte più una persona cerca di risolvere un problema apparentemente semplice, più le cose peggiorano. E si scopre che questo vale anche per le cellule: tentare di compensare ciò che inizia come una carenza o disfunzione minore può diventare un disastro.
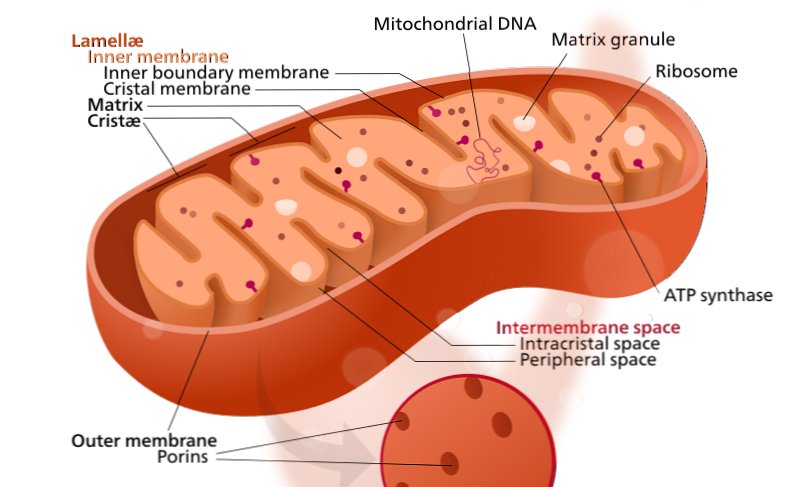
Nel caso del morbo di Alzheimer (MA), i ricercatori della Temple University ora mostrano che il rimodellamento del trasporto del calcio mitocondriale - quello che sembra essere un tentativo da parte delle cellule di compensare il calo di produzione di energia e la disfunzione metabolica - sebbene inizialmente benefico, alla fine diventa un pessimo adattamento, alimentando il declino della funzione mitocondriale, della memoria e dell'apprendimento.
La nuova ricerca, pubblicata online su Nature Communications, è la prima a collegare i cambiamenti disadattivi nel trasporto del calcio da parte dei mitocondri - i motori delle cellule che generano energia - alla progressione del MA.
"La deposizione di amiloide-beta e la patologia tau sono considerate i principali fattori che contribuiscono al MA e, di conseguenza, sono stati al centro dello sviluppo terapeutico", ha spiegato John W. Elrod PhD, professore associato della Temple e ricercatore senior del nuovo studio. "Tuttavia, grandi studi clinici che puntavano questi percorsi hanno universalmente fallito".
L'alterazione della regolazione del calcio e la disfunzione metabolica sono sospettate di contribuire alla disfunzione neuronale e allo sviluppo del MA. "Fino ad ora, nessuno ha studiato l'impatto del trasporto alterato di calcio dentro e fuori dai mitocondri sulla progressione del MA", ha osservato il dott. Elrod. "Il nostro studio attuale fornisce un collegamento mancante tra queste due ipotesi della patogenesi del MA".
Il trasporto del calcio nei mitocondri ha un ruolo importante in molte funzioni cellulari e richiede il coinvolgimento di più proteine per essere svolto con efficacia. Tra i regolatori chiave di questo processo c'è la proteina NCLX, che in precedenza il laboratorio del Dr. Elrod aveva scoperto che media l'efflusso di calcio dalle cellule cardiache. L'espressione della NCLX è anche importante nell'efflusso di calcio mitocondriale nei neuroni.
Nel loro nuovo studio, il dott. Elrod e colleghi hanno esaminato il ruolo dell'assorbimento mitocondriale di calcio da parte dei neuroni nel MA. Per fare ciò, il team ha usato un topo modello di MA familiare, in cui gli animali ospitavano tre mutazioni genetiche che danno origine a patologie che progrediscono con l'età paragonabili alla progressione del MA nei pazienti umani.
Mentre i topi portatori di tre mutazioni invecchiavano, i ricercatori hanno osservato una costante riduzione dell'espressione di NCLX. Questa riduzione è stata accompagnata da diminuzioni nell'espressione delle proteine che limitano l'assorbimento del calcio mitocondriale, con conseguente danno al sovraccarico di calcio. La perdita di NCLX è stata ulteriormente collegata all'aumento della produzione di ossidanti dannosi per le cellule.
Per comprendere meglio la rilevanza fisiologica della perdita di NCLX, il team del Dr. Elrod ha quindi eliminato completamente l'espressione di NCLX nel cervello anteriore dei topi con MA. Nei test della memoria e della funzione cognitiva, gli animali hanno mostrato alterazioni significative.
Le analisi del tessuto cerebrale di questi topi hanno mostrato che la riduzione dell'NCLX e la conseguente perdita di efflusso di calcio dai mitocondri hanno accelerato lo sviluppo dell'amiloide-beta e della patologia tau. Quando è stata ripristinata l'espressione di NCLX, i livelli di aggregati proteici dannosi sono diminuiti, l'omeostasi del calcio mitocondriale neuronale è stata ristabilita e i topi hanno recuperato dal declino cognitivo.
"I nostri risultati indicano che il rimodellamento disadattivo dei percorsi per compensare le anomalie nella regolazione del calcio, che forse hanno lo scopo di mantenere la produzione di energia nelle cellule, porta a disfunzioni neuronali e alla patologia del MA", ha affermato Elrod. "Inoltre, i nostri dati suggeriscono che l'amiloide-beta e la patologia tau si trovano effettivamente a valle della disfunzione mitocondriale nella progressione del MA, scoperta che apre un nuovo angolo terapeutico".
Il Dr. Elrod e i suoi colleghi hanno in programma di condurre un'indagine più dettagliata sulla disfunzione metabolica che si presenta prima che emerga la patologia dell'Alzheimer.
Fonte: Temple University (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Pooja Jadiya, Devin W. Kolmetzky, Dhanendra Tomar, Antonio Di Meco, Alyssa A. Lombardi, Jonathan P. Lambert, Timothy S. Luongo, Marthe H. Ludtmann, Domenico Praticò, John W. Elrod. Impaired mitochondrial calcium efflux contributes to disease progression in models of Alzheimer’s disease. Nature Communications, 29 Aug 2019, DOI
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.















 Associazione Alzheimer OdV
Associazione Alzheimer OdV