Un team di ricerca internazionale, guidato dal Consiglio Nazionale Spagnolo della Ricerca (CSIC) e da ricercatori dell'Università di Kiel e altre, ha rivelato la struttura a livello atomico dell'enzima umano peptidasi meprin β (beta).
L'enzima è legato all'infiammazione, al cancro e all'Alzheimer ed è coinvolto nella proliferazione e nella differenziazione cellulare.
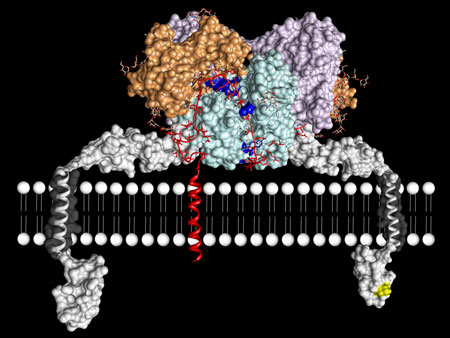 Rappresentazione grafica dell'enzima meprin β nella parete cellulare (palline bianche allineate) dove si lega a una proteina (rosso) all'interno della fessura attiva del sito (luce blu), fendendola. (Foto: Christoph Becker-Pauly & Xavier Gomis-Ruth) |
La conoscenza della struttura dell'enzima permetterà lo sviluppo di un nuovo tipo di farmaco diverso da quelli noti fino ad ora. Lo studio è stato pubblicato sull'ultimo numero della rivista Proceedings of National Academy of Sciences.
"Ora che sappiamo come si presenta il meprin β, come funziona e come si rapporta alle malattie, possiamo cercare le sostanze che bloccano le attività enzimatiche quando diventano dannose", spiega Xavier Gomis-Ruth, ricercatore dell'Istituto di biologia molecolare di Barcellona, che ha guidato il progetto.
Il meprin β è un enzima ancorato alla parete esterna delle cellule. La sua funzione normale nel metabolismo umano è tagliare alcune proteine, per esempio i fattori di crescita, che sono ancorati nella parete cellulare.
In questo modo il meprin β rilascia frammenti proteici nell'ambiente che circonda le cellule - un processo naturale e normale, finché avviene ad una certa intensità. Tuttavia, in circostanze specifiche, il meprin β può funzionare in modo anomalo, e, per esempio, rilasciare troppi frammenti proteici. I pezzi di proteine quindi esagerano il loro compito naturale nei dintorni delle cellule, causando disturbi nel corpo umano. Tale disturbo si verifica in genere quando inizia l'infiammazione, il cancro o l'Alzheimer.
Nel loro studio, gli scienziati hanno scoperto che il meprin β è composto da due molecole identiche che formano una struttura dimerica con una fenditura nel mezzo. "Abbiamo anche scoperto che la fessura attiva del sito è come la forbice dell'enzima, il luogo effettivo in cui vengono scisse le proteine", spiega il ricercatore Christoph Becker-Pauly, ricercatore dell'Istituto di Biochimica dell'Università di Kiel, e ricercatore principale del Kiel Collaborative Research Center.
Il biologo molecolare Gomes-Ruth cita il prossimo obiettivo della ricerca: "Ora abbiamo bisogno di trovare una sostanza che si adatta bene alla fessura e può quindi bloccare l'attività di scissione del meprin β". Una tale sostanza potrebbe essere la chiave per nuovi farmaci terapeutici contro l'infiammazione, il cancro o l'Alzheimer.
La ricerca è stata svolta in collaborazione con ricercatori del Max Planck Institute di Biochimica e dell'Università Johannes Gutenberg di Mainz (Germania), nonché dell'Università di Berna (Svizzera).
***********************
Cosa pensi di questo articolo? Ti è stato utile? Hai rilievi, riserve, integrazioni? Conosci casi o ti è successo qualcosa che lo conferma? o lo smentisce? Puoi usare il modulo dei commenti qui sotto per dire la tua opinione. Che è importante e unica.
***********************
Fonte: Christian-Albrechts-Universitaet zu Kiel
Riferimento: Joan L. Arolas, Claudia Broder, Tamara Jefferson, Tibisay Guevara, Erwin E. Sterchi, Wolfram Bode, Walter Stöcker, Christoph Becker-Pauly, and F. Xavier Gomis-Rüth. Structural basis for the sheddase function of human meprin β metalloproteinase at the plasma membrane. Proceedings of the National Academy of Sciences- PNAS October 2, 2012, vol. 109 no. 40 16131-1613. doi: 10.1073/pnas.1211076109.
Pubblicato in NanoWerk il 4 Ottobre 2012 - Traduzione di Franco Pellizzari.
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari proposti da Google sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.
| Sostieni l'Associazione; una donazione, anche minima, ci aiuterà ad assistere malati e famiglie e continuare ad informarti. Clicca qui a destra: |







 Associazione Alzheimer OdV
Associazione Alzheimer OdV