 Fibrinogeno umano purificato usato dallo studio (Fonte: Lori Chertoff/The Rockefeller University)
Fibrinogeno umano purificato usato dallo studio (Fonte: Lori Chertoff/The Rockefeller University)
Gli scienziati sanno da tempo che il cervello del morbo di Alzheimer (MA) spesso presenta placche e grovigli anormali, e recenti studi hanno evidenziato il ruolo del sistema vascolare del cervello nella progressione della malattia. Ma per decenni, questa conoscenza non è riuscita a tradursi in trattamenti pienamente efficaci. La mancanza di progressi è in gran parte dovuta al fatto che, nonostante grandi risultati, non è ancora chiaro il percorso preciso della neurodegenerazione.
Ora, una nuova ricerca dimostra che quando l'amiloide-beta (Aβ) si lega al fibrinogeno - una grande proteina del sangue - forma coaguli anormali che sono resistenti alla degradazione. Questi coaguli sono legati al danno e all'infiammazione vascolare e persino piccole quantità di questo complesso sembrano innescare le patologie del MA precoce, come la perdita di sinapsi, la neuroinfiammazione e l'interruzione della barriera emato -encefalica. I risultati rafforzano l'evidenza che la malattia vascolare contribuisce alla neurodegenerazione e fornisce speranza ai pazienti con MA sotto forma di un nuovo promettente bersaglio farmacologico: i complessi Aβ/fibrinogeno.
"Ci vuole una quantità maggiore di Aβ o fibrinogeno da solo per causare gravi danni nel cervello del MA", afferma Erin Norris, prof.ssa associata di ricerca nel laboratorio di Sidney Strickland alla Rockefeller University. "Ma quando i due complessi si mettono insieme, hai solo bisogno di piccole quantità di ciascuno per causare danni. C'è un effetto sinergico con Aβ e fibrinogeno".
Aggravare il problema
La laboratorio di neurobiologia e genetica di Strickland sta inseguendo il complesso Aβ/fibrinogeno da quasi due decenni. Il lavoro precedente del laboratorio ha dimostrato che l'Aβ lega il fibrinogeno e ha collegato il complesso alla patogenesi di MA. I risultati hanno suggerito una connessione tra neurodegenerazione e salute vascolare, un'affermazione una volta controversa che ha preso piede da quando il laboratorio l'ha proposta anni fa.
"Solo di recente, con una serie di scoperte sul campo, le persone hanno iniziato a credere che il sistema vascolare sia coinvolto nella patogenesi del MA", afferma la Norris. "Sin dai nostri risultati iniziali, ci siamo concentrati sullo studio dei meccanismi che spiegano come un sistema vascolare disfunzionale influisce sul MA".
Identificare il complesso Aβ/fibrinogeno è stato un buon inizio. Ma la portata del suo impatto - e se il complesso da solo potesse guidare il MA - è rimasta poco chiara. Quindi il team di Strickland ha deciso di formare il complesso a basse concentrazioni in laboratorio e introdurlo direttamente su fette di tessuto cerebrale di topo e nel cervello di topo vivi. Il loro obiettivo era isolare gli effetti di Aβ/fibrinogeno in dettaglio.
"Volevamo davvero mostrare il danno: ingrandire esattamente come si danneggiavano i terminali pre e post-sinaptici", afferma l'associata di ricerca Elisa Nicoloso Simões-Pires.
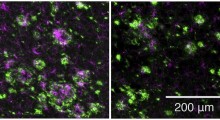
Ciò che hanno scoperto è che, sebbene ogni componente da solo, anche in quantità crescenti, non causasse molti danni, la combinazione di bassi livelli di Aβ/fibrinogeno si è dimostrata tossica per le sinapsi e ha causato molti dei tratti distintivi del MA, come la neuroinfiammazione e la rottura della barriera emato-encefalica. Hanno confermato che il complesso era responsabile usando anticorpi che hanno impedito all'Aβ di legarsi al fibrinogeno, riducendo gli effetti dannosi.
"Abbiamo dimostrato che il complesso induce effettivamente la perdita di barriera emato-encefalica, quando le sole proteine non lo hanno fatto", afferma Simões-Pires. "La rottura della barriera emato-encefalica consente alle proteine del sangue di entrare nel cervello, portando ulteriori danni".
Un nuovo obiettivo di farmaci
Uno dei punti di forza dello studio era che prevedeva sia fette cerebrali che topi vivi. "È stato un progetto in vitro e in vivo, entrambi hanno dato lo stesso esito", afferma la Norris. "Siamo molto più fiduciosi nei nostri risultati quando possiamo mostrare la stessa cosa nella cultura e in un organismo vivente". Successivamente, il team prevede di esplorare il meccanismo: perché questo complesso provoca così tanti problemi?
Potrebbero esserci anche implicazioni cliniche, poiché lo studio suggerisce che anche piccole quantità del complesso Aβ/fibrinogeno possono innescare le caratteristiche del MA molto prima che appaiano i sintomi cognitivi. I topi esposti al complesso, ad esempio, hanno mostrato anche elevati livelli di fosfo-tau181, un biomarcatore usato nell'uomo per rilevare il MA anni prima che ci siano sintomi.
Questo risultato aumenta la possibilità che l'attuale studio stia imitando le prime fasi della progressione del MA e che l'intervento precoce che punta il complesso stesso possa ritardarla o impedirla. Mentre molti meccanismi contribuiscono al MA, il team crede che questo particolare percorso meriti più attenzione.
"Non è una malattia semplice", afferma la Simões-Pires. "Molti altri fattori possono indurre la neurotossicità e certamente non proponiamo che inibire questa formazione complessa possa curare il MA. Ma forse puntare questo complesso potrebbe alleviare alcune delle patologie ed essere ancora più efficace in combinazione con altre terapie".
Fonte: Rockefeller University (> English) - Traduzione di Franco Pellizzari.
Riferimenti: E Nicoloso Simões-Pires, [+3], EH Norris. Synergistic effects of the Aβ/fibrinogen complex on synaptotoxicity, .... Alz & Dem, 2025, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.
Rockefeller University






 Associazione Alzheimer OdV
Associazione Alzheimer OdV