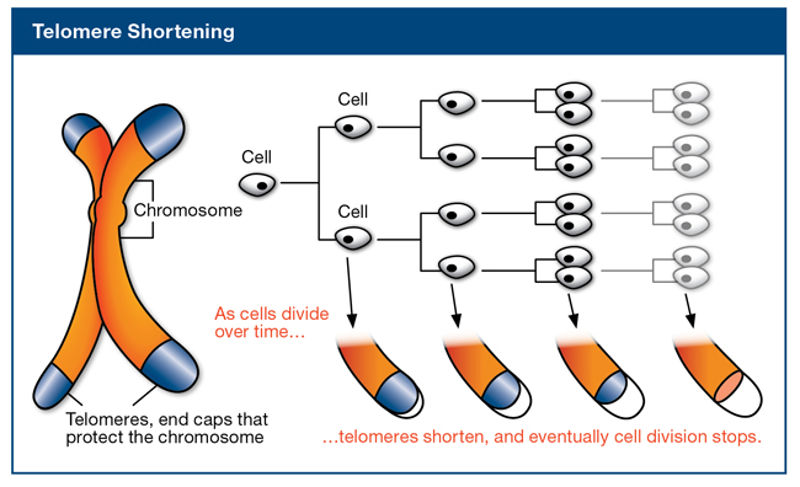
 A ogni suddivisione della cellula, i telomeri (cappucci all'estremità dei cromosomi) si accorciano e alla fine cessa la suddivisione.
A ogni suddivisione della cellula, i telomeri (cappucci all'estremità dei cromosomi) si accorciano e alla fine cessa la suddivisione.
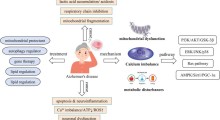
Gli scienziati sanno molto delle caratteristiche dei diversi tipi di demenza. Il morbo di Alzheimer (MA) è caratterizzato da accumuli di proteine amiloidi e tau. La demenza vascolare è il risultato di vasi sanguigni rotti e nodosi che di norma forniscono ossigeno al cervello. Il Parkinson e altre forme di demenza a corpi di Lewy sono causate da proteine alfa-sinucleina deformi nel cervello.
La saggezza popolare vuole che ciascuna di queste demenze abbia bisogno di un proprio trattamento. Un farmaco anti-amiloide probabilmente non funzionerà per qualcuno che non ha accumuli di amiloide nel cervello.
Ma a tutt'oggi non ci sono trattamenti definitivi, o misure preventive, per una qualsiasi delle decine di demenze esistenti. Fatto che ha portato alcuni ricercatori ad adottare un approccio più sistematico: e se ci fosse un unico meccanismo nel cervello che, quando difettoso, porta a tutte le forme di demenza? E se questo meccanismo, come un interruttore, potesse essere invertito?
Questo è il pensiero di Michael Fossel, il fondatore della nuova azienda di biotecnologie Telocyte fondata nel 2015 in Michigan, che sta sviluppando terapie per il MA. Martedì scorso, 14 gennaio, Fossel ha pubblicato uno studio di revisione che postula che il MA e altre forme di demenza sono causati dal fallimento delle cellule cerebrali, gran lavoratrici, chiamate glia. E propone, inoltre, una soluzione: una terapia genica che potrebbe puntare queste cellule per tenere a bada la demenza.
La ricerca è teorica: è una revisione, quindi non presenta dati originali. È un nuovo modo di pensare, una proposta audace. “È incoraggiante vedere persone come il dott. Fossel mettere insieme ricerche e cercare di arrivare a nuove teorie”, dice Rebecca Edelmayer, direttrice dell'impegno scientifico dell'Alzheimer's Association, ente senza scopo di lucro, editrice di Alzheimer's and Dementia, la rivista dove è apparsa la revisione di Fossel.
Ma anche se le teorie sono importanti, dice la Edelmayer, “devono comunque essere testate”. Le terapie geniche sono ancora relativamente nuove. E non c'è motivo di farsi domande sulla sicurezza genetica che introdurrebbe la terapia: una che codifica l'enzima telomerasi. Prima che gli scienziati possano anche cominciare a testare la teoria sistematica di Fossel sulla demenza, avranno bisogno di molti dati che dimostrano la sua sicurezza.
Conviene studiare il telomerasi per la demenza?
Il telomerasi è al centro della ricerca sulla longevità da anni. Si tratta di un enzima che allunga i telomeri, che sono i tappi genetici alle estremità dei cromosomi. Ogni volta che una cellula si divide, i telomeri si accorciano, e quando i telomeri sono sufficientemente erosi, le cellule entrano in uno stato chiamato 'senescenza', smettono di dividersi e si auto-distruggono.
Telomeri più corti sono stati correlati con tutta una serie di problemi di salute legati all'età: cancro, diabete e anche varie forme di demenza. Ma non sono i telomeri stessi che causano questi problemi, Fossel suggerisce: “Come i miei telomeri si accorciano, ci sono anche molte altre cose che avvengono”.
La lunghezza relativa dei telomeri, sappiamo, invia un segnale al resto del DNA della cellula. Mentre i telomeri si accorciano con la replicazione cellulare, le cellule cambiano il modo di eseguire altre istruzioni genetiche, con una possibile produzione non corretta di proteine. È un processo chiamato 'effetto positrone del telomero' (telomere positron effect), che gli scienziati ancora non capiscono del tutto.
Fossel postula che quando i telomeri si accorciano nelle cellule microglia (parte del sistema immunitario del cervello), si degradano anche altre parti critiche del loro DNA, e quel danno genetico può provocare molte demenze diverse.
La terapia genica di Telocyte avrebbe lo scopo di ricostruire i telomeri gliali. Ciò comporterebbe l'invio di una copia attiva del gene telomerasi (TERT) nel liquido cerebrospinale, portata da un virus. Il virus, che dovrebbe essere altrimenti benigno, non va bene per portare materiale genetico in cellule specifiche: in topi modello, circa il 5% del totale della terapia va a finire nei neuroni, senza alcun effetto duraturo, e circa l'1% finisce nelle microglia, secondo Fossel. Ma anche se il gene TERT resta intorno alla cellula gliale per un paio di settimane o mesi, potrebbe essere sufficiente al telomerasi per allungare quei tappi terminali e indurre la cellula ad esprimere i geni come quando era giovane.
Di solito, le terapie geniche funzionano introducendo nuovo materiale genetico che sostituisce il codice genetico difettoso o mancante di una persona. La terapia genica di Telocyte, tuttavia, non sostituirebbe geni: darebbe solo alle cellule gliali un'altra copia di un gene che già hanno. Tutte le nostre cellule hanno il gene TERT incorporato nei cromosomi. Ma la stragrande maggioranza delle cellule (tranne che globuli rossi, spermatozoi o ovuli, e le cellule lungo le parti del tubo digerente) hanno il gene spento in permanenza.
Questo è per una buona ragione: il telomerasi è attivo nella maggior parte delle forme di cancro. È per questo che molti scienziati temono che l'inserimento di un gene che codifica il telomerasi (come intende fare la terapia genica di Telocyte) rischi di causare il cancro
“La mia preoccupazione principale è la sua sicurezza”, dice Jue Lin, biologa molecolare dell'Università della California di San Francisco, il cui lavoro si concentra sullo studio dei livelli di lunghezza e stress dei telomeri nel tempo. “Non sappiamo se la sovra-espressione del telomerasi aumenta il rischio di cancro”. Nel cervello, in particolare nelle cellule gliali che la terapia genica proposta di Fossel dovrebbe puntare, il tumore in questione sarebbe probabilmente un glioblastoma, un tumore cerebrale che cresce voracemente.
I topi modello che hanno avuto la terapia genica del telomerasi nel cervello hanno mostrato effetti promettenti, senza incidenza notevole di cancro, ma questi esperimenti sono imperfetti. I topi esprimono la telomerasi in modo diverso dagli esseri umani, spiega la Lin: "Hanno molto più telomerasi, in più tessuti, rispetto ad esseri umani. I topi non vivono nemmeno a lungo come noi, e il cancro richiede molto tempo per svilupparsi".
E terapie geniche comportano il rischio di una reazione immunitaria pericolosa contro il virus che trasporta il gene terapeutico. I virus usati nella terapia genica oggi, e quello che Fossel propone di usare, dovrebbero essere più sicuri di quelli usati nei primi giorni della terapia genica. Il virus adeno-associato (AAV) dovrebbe suscitare solo la più piccola delle risposte immunitarie. Ma di recente gli scienziati hanno espresso preoccupazioni circa la sicurezza a lungo termine delle terapie geniche che usano l'AAV.
Vale la pena correre questo rischio?
Tenuto conto dei rischi, non c'è accordo sul fatto che valga la pena perseguire l'approccio telomerasi. “È importante e interessante avere un'ipotesi ulteriore”, dice Diego Forero, ricercatore della Fondazione Universitaria dell'Área Andina in Colombia. Il suo lavoro, che è indipendente da quello di Fossel, si concentra sull'esposizione degli astrociti (un tipo di cellule gliali del cervello) al telomerasi, per vedere come reagiscono. Ha scoperto che il telomerasi è coinvolto in altre funzioni cellulari, come il metabolismo della cellula. A suo parere, è troppo presto per dire che la teoria di Fossel deve essere testata.
Piuttosto che concentrarsi sull'applicazione terapeutica potenziale del telomerasi nelle cellule cerebrali, Forero è interessato alla ricerca più di base, esplorativa. Pensa che applicarla ad un determinato obiettivo, come una cura per la demenza, non direbbe granché agli scienziati su tutti i modi in cui il telomerasi potrebbe influenzare le cellule cerebrali.
Quegli inviti alla prudenza possono essere frustranti per i pazienti con demenza, vista la scarsità di opzioni. Anche senza avere piani immediati per condurre studi clinici, Fossel dice che è stato contattato da circa 200 persone con demenza lieve o moderata, che si sono proposti come partecipanti volontari. Questi sono ammissibili alla maggior parte degli altri studi clinici su terapie per la demenza, che tendono a cercare partecipanti con fattori di rischio della malattia, ma con sintomi minimi, o del tutto assenti.
“Le persone hanno di fronte una malattia terribile e dicono «Voglio prendermi i rischi»”, dice Arthur Caplan, bioetico del Langone Medical Center della New York University. Con le popolazioni vulnerabili alla disperata ricerca di un trattamento, diventa ancora più importante il controllo dei pari da parte di scienziati indipendenti. È fondamentale che i dati e la ricerca siano gestiti da soggetti che non hanno un interesse finanziario investito in un certo esito.
Questi studi hanno anche bisogno di avere forti comitati di revisione istituzionali, Caplan dice. Questi comitati sono richiesti ogni volta che i ricercatori conducono esperimenti con soggetti umani, specialmente quando i rischi sono così alti.
La Libella Gene Therapeutics, una startup biotech del Kansas, sta iniziando quest'anno uno studio clinico con la terapia genica del telomerasi per trattare l'invecchiamento generico. Tuttavia, sta svolgendo il lavoro in Colombia, dove gli standard per i comitati di revisione istituzionale non sono così stringenti come negli Stati Uniti. È una tattica informalmente conosciuta come 'IRB shopping' e fa sollevare le sopracciglia nella comunità di ricerca.
“Siamo sempre aperti a nuove idee e nuovi modi per trattare la demenza”, dice la Edelmayer. “Non dobbiamo lasciare nulla di intentato”. Ma, ha continuato, "le cose più grandi che vogliamo vedere non devono essere solo teorie. Noi vogliamo vederle provate”.
Fonte: Katherine Ellen Foley in Quartz (> English text) - Traduzione di Franco Pellizzari.
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.








 Associazione Alzheimer OdV
Associazione Alzheimer OdV