 Vedi l'animazione di Nalini Rao qui
Vedi l'animazione di Nalini Rao qui
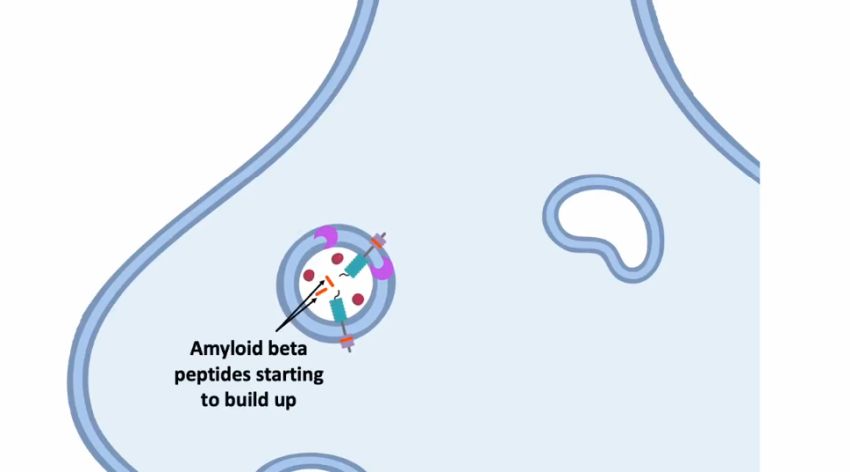
Sebbene medici e scienziati sappiano da tempo che il morbo di Alzheimer (MA) comporta l’accumulo di frammenti proteici tossici nel cervello, hanno faticato a capire come vengono prodotti questi frammenti dannosi. Ora, in un nuovo studio pubblicato su Science Translational Medicine, scienziati della Northwestern University di Evanston (Illinois/USA) hanno individuato quando e dove le proteine tossiche si accumulano nel cervello dei pazienti con MA e hanno trovato un farmaco approvato dalla FDA vecchio di decenni che può fermare il processo di accumulo prima ancora che inizi.
Studiando modelli animali, neuroni umani e tessuto cerebrale di pazienti ad alto rischio, il team ha scoperto un frammento proteico particolarmente tossico, chiamato amiloide-beta42 (Aβ42), che si accumula all’interno delle vescicole sinaptiche dei neuroni, i minuscoli pacchetti che i neuroni usano per inviare segnali. Ma, quando gli scienziati hanno somministrato il levetiracetam (un farmaco antiepilettico poco costoso, vecchio di decenni) agli animali e ai neuroni umani, il farmaco ha impedito ai neuroni di formare Aβ42.
"Mentre molti dei farmaci per il MA attualmente sul mercato, come lecanemab e donanemab, sono approvati per eliminare le placche amiloidi esistenti, abbiamo identificato questo meccanismo che impedisce la produzione dei peptidi Aβ42 e le placche amiloidi", ha detto l'autore senior Jeffrey Savas, professore associato di neurologia comportamentale alla Northwestern University. “Abbiamo scoperto una nuova biologia e allo stesso tempo aperto le porte a nuovi bersagli farmacologici”.
Introduzione dei farmaci antiepilettici nella lotta al MA
Al centro della nuova scoperta c’è la proteina precursore dell’amiloide (APP), una proteina con un ruolo importante nello sviluppo del cervello e nella formazione sinaptica. L’elaborazione anormale dell’APP può portare alla produzione di peptidi Aβ, che hanno un ruolo centrale nello sviluppo del MA. Gli scienziati della Northwestern hanno scoperto che il modo in cui l’APP viene trafficata controlla anche se un neurone forma Aβ42.
Durante il ciclo delle vescicole sinaptiche – un processo fondamentale che è alla base di ogni pensiero, movimento, memoria o sensazione – il levetiracetam si lega a una proteina chiamata SV2A. Questa interazione rallenta una fase in cui i neuroni riciclano i componenti della vescicola sinaptica dalla superficie della cellula. Interrompendo questo processo di riciclaggio, il farmaco consente all’APP di rimanere sulla superficie della cellula più a lungo, allontanandola dal percorso che produce le proteine tossiche Aβ42.
"A 30, 40 e 50 anni, il nostro cervello è generalmente in grado di allontanare le proteine dai percorsi dannosi", ha detto Savas. "Con l'avanzare dell'età, quella capacità protettiva si indebolisce gradualmente. Questa non è una dichiarazione di malattia; è solo una parte dell'invecchiamento. Ma nel cervello che sviluppa il MA, troppi neuroni vanno fuori strada, ed è allora che inizia la produzione di Aβ42. E poi c'è la tau (o 'grovigli'), e poi ci sono le cellule morte, poi la demenza, poi la neuroinfiammazione ... e poi è troppo tardi".
Il farmaco dovrebbe essere assunto “molto, molto presto”
Per prevenire efficacemente i sintomi del MA, gli individui ad alto rischio dovrebbero iniziare a prendere il levetiracetam "molto, molto presto", ha detto Savas, forse fino a 20 anni prima che il nuovo test sul MA approvato dalla FDA possa rilevare livelli leggermente elevati di Aβ42.
"Non dovresti prenderlo quando hai già la demenza perché il cervello ha già subito una serie di cambiamenti irreversibili e molta morte cellulare", ha detto Savas.
Per questo motivo, Savas ha detto che lui e il suo team potrebbero tentare di identificare popolazioni di pazienti con forme genetiche di MA, che includono pazienti con sindrome di Down. Sebbene questi pazienti siano piuttosto rari, rappresentano il gruppo chiave che trarrà beneficio da queste scoperte.
Estrazione di dati clinici umani esistenti
Sfruttando il suo stato di farmaco approvato dalla FDA e ampiamente impiegato, il team ha estratto i dati clinici umani esistenti per indagare se i pazienti con MA che assumevano levetiracetam presentavano un rallentamento del declino cognitivo. Hanno ottenuto dati clinici dal Centro Nazionale Coordinamento Alzheimer e hanno condotto un'analisi correlativa, scoprendo che i pazienti con MA che assumevano levetiracetam erano associati a un ritardo significativo dalla diagnosi di declino cognitivo alla morte rispetto a quelli che assumevano lorazepam o nessun/altro farmaco antiepilettico.
"Sebbene l'entità del cambiamento sia stata piccola (nell'ordine di pochi anni), questa analisi supporta l'effetto positivo del levetiracetam nel rallentare la progressione della patologia di MA", ha detto Savas.
Lo studio ha esaminato anche il cervello della sindrome di Down
Oltre a usare topi modello geneticamente modificati e colture di neuroni umani, gli scienziati hanno anche studiato il tessuto cerebrale umano di pazienti deceduti con sindrome di Down, morti tra i 20 ei 30 anni a causa di incidenti stradali o altri eventi. Oltre il 95% dei pazienti con sindrome di Down sviluppa una forma precoce e aggressiva di MA intorno ai 40 anni, ha detto Savas, perché il gene APP è collegato al cromosoma che è triplicato nel loro genoma.
"Ottenendo cervelli di pazienti con sindrome di Down da persone morte tra i 20 ei 30 anni, sappiamo che avrebbero infine sviluppato l'Alzheimer, quindi questo ci dà l'opportunità di studiare i primissimi cambiamenti iniziali nel cervello umano", ha detto Savas. Lo studio ha scoperto che questi cervelli avevano lo stesso accumulo di proteine presinaptiche che il laboratorio di Savas aveva trovato nei topi modello progettati in uno studio precedente.
"Questo è ciò che noi e altri chiamiamo lo 'stadio paradossale' del MA, ovvero prima che le sinapsi si perdano e ne consegua la demenza, la prima cosa che accade è l'accumulo di proteine presinaptiche", ha detto Savas. "Quindi plausibilmente, se si iniziasse a somministrare a questi pazienti il levetiracetam durante l'adolescenza, si potrebbe effettivamente avere un beneficio terapeutico preventivo".
Savas ha affermato che il levetiracetam “non è perfetto” e ha osservato che il farmaco si decompone nel corpo molto rapidamente. Lui e altri hanno iniziato a creare una versione migliore del levetiracetam, che durerebbe più a lungo nel corpo e aiuterebbe a colpire meglio il meccanismo che impedisce la produzione delle placche.
Fonte: Northwestern University (> English) - Traduzione di Franco Pellizzari.
Riferimenti: NR Rao, [+15], JN Savas. Levetiracetam prevents Aβ production through SV2a-dependent modulation of APP processing in Alzheimer’s disease models. Sci Trans Med, 2026, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.







 Associazione Alzheimer OdV
Associazione Alzheimer OdV