Un team di ricerca dell'Università di Barcellona (UB) ha scoperto nuovi meccanismi molecolari legati al declino cognitivo associato al morbo di Alzheimer (MA), descrivendo per la prima volta il ruolo decisivo della proteina RTP801 negli astrociti durante la progressione della malattia.
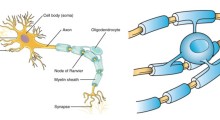
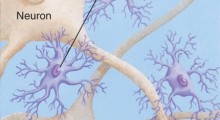
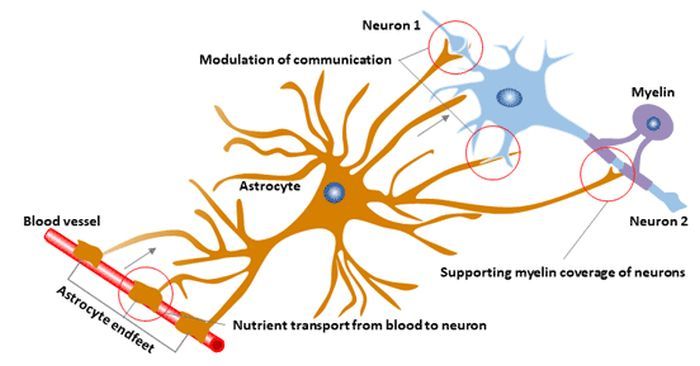 Funzioni degli astrociti tra i neuroni e i capillari nel cervello (Fonte: Cusabio)
Funzioni degli astrociti tra i neuroni e i capillari nel cervello (Fonte: Cusabio)
Nel MA, che non ha ancora una cura, esiste un accumulo di placche di amiloide-beta (Aβ) al di fuori dei neuroni, e di grovigli di proteine tau iperfosforilate all'interno dei neuroni. La proteina RTP801, codificata dal gene DDIT4 nei neuroni dell'ippocampo, è coinvolta nel processo di neuroinfiammazione, neurotossicità e progressione della malattia, come dettagliato dal team in un studio precedente (Cell Death and Disease, 2021).
Come in altre malattie che alterano la funzione cerebrale e causano la morte cellulare, questa patologia comporta un'interazione complessa tra diversi tipi di cellule nel sistema nervoso centrale. Ora, il nuovo studio descrive per la prima volta il ruolo cruciale della proteina RTP801 negli astrociti, cellule cerebrali specifiche coinvolte nella neuroinfiammazione, nella regolazione sinaptica e nell'omeostasi cerebrale.
"Gli astrociti, in precedenza considerati cellule di supporto passivo, agiscono come regolatori attivi dei processi neurodegenerativi, incluso il mantenimento dell'equilibrio eccitatorio-inibitorio e le risposte neuroimmuni. La RTP801 è una proteina di risposta allo stress coinvolta nella disfunzione neuronale, ma il suo ruolo specifico negli astrociti non era noto", ha detto Cristina Malagelada, autrice senior dello studio pubblicato su Alzheimer's & Dementia.
Usando tecniche di terapia genica, il team ha esplorato gli effetti del silenziamento dell'espressione della proteina RTP801 negli astrociti dell'ippocampo dorsale di animali modello della malattia. Lo studio ha analizzato l'impatto del silenziamento genico sulla memoria spaziale, sugli interneuroni positivi alla parvalbumina (PV+) e sulla connettività cerebrale funzionale, che sono interconnessi dalla funzione dei circuiti neurali inibitori.
"Nel MA, la disfunzione di questi circuiti porta a compromissione cognitiva, disregolazione emotiva e interruzione dell'attività della rete cerebrale, che sono aspetti chiave della progressione della malattia. Inoltre, abbiamo anche esaminato la sua influenza sui marcatori neuroinfiammatori, in particolare l'astrogliosi, la microgliosi e l'attivazione di inflammazione", spiega Almudena Chicote, prima autrice dello studio.
Secondo lo studio, quando i livelli di RTP801 sono ridotti negli astrociti dell'animale modello di MA, diminuisce anche l'iperconnettività di queste reti cerebrali. Pertanto, normalizzare l'espressione di RTP801 aiuterebbe a ripristinare la connettività della rete cerebrale come quella di individui sani.
Cambiamenti metabolici e neurali
Il team ha anche scoperto che i livelli di GABA - un neurotrasmettitore essenziale per inibire l'eccitabilità cerebrale - sono ridotti negli animali modello di MA. Tuttavia, questa condizione può essere parzialmente invertita quando viene silenziata l'espressione della proteina RTP801 negli astrociti. Questi cambiamenti metabolici sono stati collegati alla perdita di un tipo specifico di interneuroni PV+ che sintetizzano il GABA nell'ippocampo.
"Pertanto, il silenziamento della proteina RTP801 può aiutare a invertire parte del danno agli interneuroni PV+ nell'ippocampo, e questo potrebbe aiutare a ripristinare un'adeguata produzione di GABA e migliorare la funzione cerebrale", osserva Almudena Chicote.
Lo studio suggerisce anche che la connettività aberrante della rete cerebrale - l'iperconnettività o aumento dell'attività della rete cerebrale - osservata in alcuni modelli potrebbe essere spiegata dalla tossicità della proteina RTP801 nei neuroni PV+ nell'ippocampo, che sono produttori chiave di GABA. "La riduzione di RTP801 ha parzialmente ripristinato questi neuroni e ha migliorato i livelli di GABA", afferma la ricercatrice.
Il team prevede di espandere le linee di ricerca per rafforzare i risultati in vitro e convalidare l'uso del silenziamento della proteina RTP801 nelle future strategie terapeutiche per affrontare il MA.
Fonte: Universitat de Barcelona (> English) - Traduzione di Franco Pellizzari.
Riferimenti: A Chicote-González, [+9], C Malagelada. Astrocytes, via RTP801, contribute to cognitive decline by disrupting GABAergic-regulated connectivity and driving neuroinflammation in an Alzheimer's disease mouse model. Alz&Dem, 2025, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.





 Associazione Alzheimer OdV
Associazione Alzheimer OdV