Il controllo di qualità dell'mRNA è stato identificato come nuovo obiettivo di farmaci per l'Alzheimer e le demenze correlate.
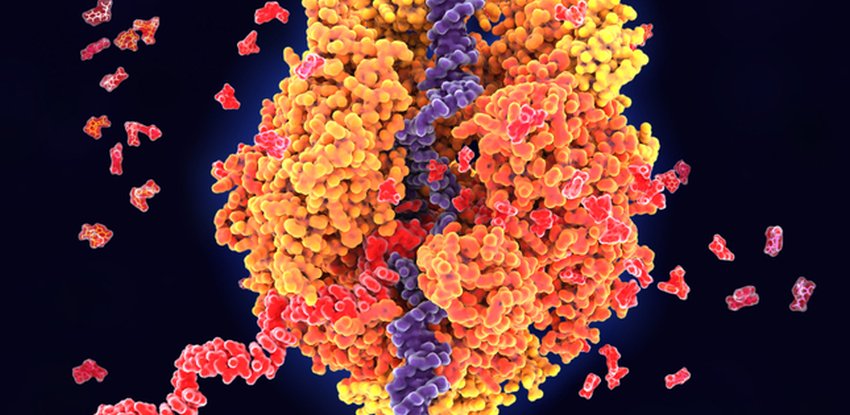
I ricercatori dell'Università del Texas di San Antonio (UT Health San Antonio) hanno comunicato su Alzheimer's & Dementia la scoperta di un nuovo meccanismo con cui le forme patologiche della proteina tau causano la morte dei neuroni.
Il morbo di Alzheimer (MA) e l'encefalopatia traumatica cronica (CTE) sono alcuni dei più di 20 disturbi che includono la patologia della proteina tau. Il meccanismo del danno indotto dalla tau appena scoperto può essere alterato farmacologicamente, secondo gli scienziati, rendendolo un nuovo obiettivo per lo sviluppo di farmaci.
"La ricerca fornisce un quadro per studi futuri nei modelli vertebrati di taupatia e alla fine per studi clinici nelle persone", ha detto la prima autrice Gabrielle Zuniga, dottoranda della UT Health San Antonio. "Il fatto che sia un bersaglio colpibile con farmaci è davvero interessante, ed è un nuovo meccanismo che non era stato fissato in precedenza".
Un evento precoce, prima che muoiano i neuroni
Lavorando con moscerini della frutta che esprimono tau umana mutante, gli scienziati hanno osservato i deficit in un percorso di controllo della qualità dell'RNA chiamato nonsense-mediated mRNA decay (decadimento di mRNA mediato da nonsense). La Zuniga spiega:
"Questo è un evento precoce, questi cambiamenti nel controllo di qualità dell'RNA si verificano molto prima della morte della cellula neuronale. Il nonsense-mediated mRNA decay è un passo fondamentale nel processo attraverso il quale le informazioni genetiche sono tradotte in proteine.
"Il deterioramento di questo meccanismo di controllo di qualità provoca l'accumulo di RNA e la produzione di proteine disfunzionali anormali, un effetto assolutamente dannoso".
Il DNA (DeoxyriboNucleic Acid, acido desossiribonucleico o deossiribonucleico) contiene le matrici genetiche delle proteine, mentre l'RNA (RiboNucleic Acid, acido ribonucleico) messaggero (mRNA) legge tali matrici, creando le proteine. Questa autostrada informativa si ingorga quando il nonsense-mediated mRNA decay è ridotto.
"Ci stiamo concentrando sul modo in cui le cellule puliscono l'RNA difettoso e come questo meccanismo di controllo della qualità dell'RNA va male nelle malattie. Se questi tipi di RNA si accumulano in una cellula e sono tradotti in proteine, possono accadere cose pessime", ha detto l'autrice senior Bess Frost PhD, prof.ssa distinta di ricerca nei disturbi neurodegenerativi dell'UT Health San Antonio, nonché prof.ssa associata di sistemi cellulari e anatomia.
Andare oltre la deposizione di tau
I trattamenti per il MA e le altre taupatie sono falliti in parte perché si sono concentrati sull'eliminazione della proteina tau o dell'altra chiamata amiloide-beta: le placche di amiloide-beta e i grovigli di tau sono caratteristiche classiche del MA.
"Piuttosto che puntare la deposizione di tau, che viene tardi nel corso della malattia, perché non fermiamo i percorsi che stanno effettivamente facendo morire i neuroni?" ha detto Sudha Seshadri MD, prof.ssa di neurologia della facoltà di medicina e direttrice fondatrice del Glenn Biggs Institute. "Questo sembra essere uno di quei sentieri, e la sua scoperta è un pezzo brillante di lavoro investigativo di Gabrielle Zuniga, della dott.ssa Frost e della squadra".
L'identificazione dei diversi meccanismi sottostanti la patologia tau (e amiloide-beta) potrebbe farci capire quali pazienti potrebbero beneficiare di quali terapie, ha detto Nicolas Musi MD, professore di medicina dell'UT Health San Antonio e direttore del Sam e Ann Barshop Institute. Ad esempio, un sottoinsieme dei pazienti con MA potrebbe essere reattivo a un farmaco che aumenta il nonsense-mediated mRNA decay.
Fonte: Will Sansom in University of Texas Health (> English) - Traduzione di Franco Pellizzari.
Riferimenti: Gabrielle Zuniga, S Levy, P Ramirez, J De Mange, E Gonzalez, M Gamez, Bess Frost. Tau‐induced deficits in nonsense‐mediated mRNA decay contribute to neurodegeneration. Alzheimer's & Dementia, 2022, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.





 Associazione Alzheimer OdV
Associazione Alzheimer OdV