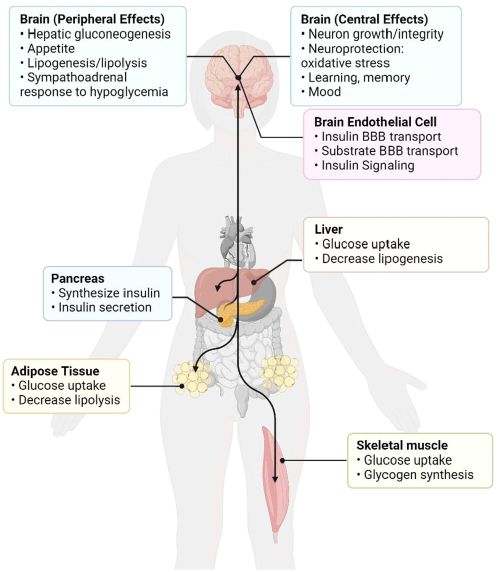
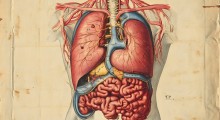
 Azioni (frecce nere) dell'insulina in periferia e nel cervello. L'insulina (sintetizzata in gran parte dal pancreas) attraversa la barriera emato-encefalica (BBB) per agire all'interno del sistema nervoso centrale e regolare sia gli effetti diretti all'interno del cervello che gli eventi di segnalazione indiretta che si riflettono sulla periferia. I suoi ruoli sono molto vari e possono riflettere la sua storia evolutiva come regolatore di crescita. Nella periferia, l'insulina influenza tutti i tessuti, ma colpisce principalmente quelli metabolici, come il tessuto adiposo, il fegato e il muscolo scheletrico. (Fonte: Schwartz et al / Neuroprotection)
Azioni (frecce nere) dell'insulina in periferia e nel cervello. L'insulina (sintetizzata in gran parte dal pancreas) attraversa la barriera emato-encefalica (BBB) per agire all'interno del sistema nervoso centrale e regolare sia gli effetti diretti all'interno del cervello che gli eventi di segnalazione indiretta che si riflettono sulla periferia. I suoi ruoli sono molto vari e possono riflettere la sua storia evolutiva come regolatore di crescita. Nella periferia, l'insulina influenza tutti i tessuti, ma colpisce principalmente quelli metabolici, come il tessuto adiposo, il fegato e il muscolo scheletrico. (Fonte: Schwartz et al / Neuroprotection)
I percorsi della glucoregolazione cerebrale e dell'insulina sono stati finora difficili da studiare. Nuovi approcci hanno dimostrato che, all'interno del cervello, la regolazione del glucosio opera in un 'microsistema' semiautonomo distinto da quello della glucoregolazione in periferia. Come in periferia, tuttavia, nel cervello può verificarsi una disglicemia perniciosa.
La glucolipotossicità è ampiamente legata all'emorragia nella vascolarizzazione cerebrale, al danno microvascolare, all'accumulo di peptide amiloide-β e al danno strutturale. Nell'ambiente energetico localizzato del cervello, l'iperglicemia, l'iperinsulinemia e la resistenza all'insulina costituiscono fattori di rischio indipendenti per il morbo di Alzheimer (MA).
Ora è stato dimostrato che la glucolipotossicità interferisce con il reticolo endoplasmatico e la funzione mitocondriale, provoca compromissione e danni strutturali a proteine, lipidi e acidi nucleici e rompe l'omeostasi redox, tutti fattori che contribuiscono al danno ai neuroni e alle cellule gliali.
I disturbi nella barriera emato-encefalica (BBB) e la resistenza all'insulina cerebrale sono altri insulti cruciali e di recente comprensione nel MA causati dalla disglicemia. Questi risultati di ricerca provengono dai laboratori di Elizabeth M Rhea e William A Banks della University of Washington di Seattle, coautori dello studio di revisione pubblicato su Neuroprotection.
Sebbene la traslazione di queste intuizioni alla pratica clinica per la funzione e la disfunzione cerebrale sia relativamente emergente, i risultati di studi sul diabete stanno portando a incorporare nuovi standard nella prescrizione di cure di routine. Importanti studi clinici hanno dimostrato che i trattamenti per abbassare il glucosio nei pazienti con diabete di tipo 2 (T2D) possono ridurre il rischio di sviluppare MA. Ciò ha portato l'American Diabetes Association (ADA) a elevare i problemi cognitivi (o il loro rischio) come comorbidità all'interno dei piani di trattamento dei pazienti T2D.
"I fattori di rischio e la neuropatologia del declino cognitivo e l'insorgenza e la progressione dei disturbi legati alla demenza erano fumosi, fino a poco tempo fa", afferma il dott. Stanley S. Schwartz MD, primo autore. "Il dismetabolismo del glucosio è un fattore critico di predisposizione alla demenza, compreso il MA. La disglicemia cerebrale blocca la segnalazione dell'insulina, un meccanismo altrimenti potenzialmente protettivo contro le placche del MA".
"I trattamenti cardiovascolari e del diabete - approcci che affrontano l'asse cardiorenale - sono migliorati nel corso dei decenni. Questi stanno permettendo alle persone di vivere più a lungo con questa malattia, abbastanza a lungo da diventare a rischio di complicanze legate all'età come MA e demenza", aggiunge la dott.ssa Mary E. Herman PHD, coautrice della revisione.
Queste prove influenzano drasticamente il trattamento preferito dei medici per i pazienti con T2D e problemi cognitivi comorbidi o per quelli a rischio. Lo standard aggiornato per la terapia di riduzione del glucosio include la metformina, gli inibitori della dipeptidyl peptidasi-4, gli agonisti del recettore peptide-1 tipo-glucagone e gli inibitori del cotrasporter-2 di sodio-glucosio, agenti che non solo riducono la resistenza all'insulina ma hanno anche dimostrato di rallentare lo sviluppo e/o la progressione del MA.
Al contrario, le sulfoniluree sono un'opzione meno favorevole per preservare la funzione cognitiva e l'uso di insulina iniettata dovrebbe essere riconsiderato come strategia di trattamento di prima linea o di lungo termine. L'impatto differenziale dei singoli agenti di riduzione del glucosio sulla funzione e sull'integrità neuronale può aiutare a chiarire l'interazione tra omeostasi del glucosio e salute neurale.
Studi su larga scala hanno rivelato inaspettatamente che classi specifiche di agenti antidiabetici presentano azioni pleiotropiche distinte. Questi agenti mostrano vantaggi selettivi per i sistemi di organi compromessi dal diabete, in particolare la funzione cognitiva. Sfruttare queste proprietà pleiotropiche vantaggiose può guidare il futuro sviluppo razionale di terapie contro il MA e il declino cognitivo. Approcci promettenti includono formulazioni progettate per una maggiore penetrazione cerebrale, come gli agonisti intranasali dell'incretina che bypassano la BBB. Gli agonisti del recettore dell'incretina mitigano anche la neuroinfiammazione deleteria attraverso meccanismi ancora da identificare.
Fonte: Chinese Medical Journals via EurekAlert! (> English) - Traduzione di Franco Pellizzari.
Riferimenti: SS Schwartz, ]+2], ME Herman. Beta cells to brain cells: the pivotal role of insulin and glucose metabolism in Alzheimer's disease. Neuroprotection, 2025, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.



 Associazione Alzheimer OdV
Associazione Alzheimer OdV