 Image by viarprodesign on Freepik
Image by viarprodesign on Freepik
Ieri (10 giungo 2024) un gruppo indipendente di esperti ha raccomandato all'unanimità l'approvazione della FDA dell'anticorpo monoclonale anti-amiloide donanemab. Penso che sia molto probabile che l'approvazione FDA completa sia imminente. Il donanemab sembra essere efficace almeno quanto il lecanemab già approvato nel rimuovere l'amiloide-beta (Aβ) dal cervello e rallentare modestamente il tasso di declino cognitivo nei pazienti con lieve compromissione cognitiva e demenza da morbo di Alzheimer (MA) precoce.
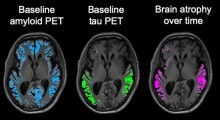
In alcuni pazienti, i biomarcatori di Aβ come le scansioni PET amiloide sono diminuiti al di sotto della soglia di rilevamento, consentendo di fermare il trattamento. Non è ancora noto se le placche Aβ alla fine torneranno e richiederanno un trattamento aggiuntivo. Va sottolineato che nonostante la rimozione completa di placche Aβ rilevabili, il donanemab rallenta ma non blocca di progressione della compromissione cognitiva.
Dubito che la rimozione di Aβ da sola risulterà mai in una cura per il MA una volta che la compromissione cognitiva è evidente. Un indizio che suggerisce una via da seguire è la constatazione che i soggetti con accumulo minimo di proteina tau sulle scansioni PET avevano la risposta più robusta al donanemab. Questi farmaci sembrano funzionare meglio nelle prime fasi del MA. Attualmente sono in corso studi per esaminare gli effetti di donanemab e lecanemab nella prevenzione della demenza in soggetti pre-sintomatici che hanno già placche amiloidi nel cervello. I risultati ci saranno tra diversi anni.
E la sicurezza? Sia donanemab che lecanemab possono causare effetti collaterali potenzialmente mortali chiamati ARIA (amyloid-related imaging abnormalities, anomalie di scansione correlate all'amiloide). Di solito questi sono lievi e spesso senza sintomi, ma in casi rari possono causare gonfiore e/o sanguinamento potenzialmente letali nel cervello. Tre soggetti nell'esperimento del donanemab sono morti per queste gravi risposte al farmaco. È molto più probabile che le ARIA gravi si verifichino in soggetti con due copie dell'allele ApoE-4.
Secondo me, come neurologo in pensione con due copie di APOE-4, che ha trascorso due giorni in terapia intensiva con ARIA grave durante lo studio sull'aducanumab, gli anticorpi monoclonali anti-amiloide dovrebbero essere usati solo con estrema cautela e frequente monitoraggio via risonanza magnetica (RM) in quelli con due copie di ApoE-4 o in quelli con prove di angiopatia cerebrale alla RM.
Fonte: Daniel Gibbs in A Tattoo On My Brain (> English) - Traduzione di Franco Pellizzari.
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.




 Associazione Alzheimer OdV
Associazione Alzheimer OdV