Negli ultimi dieci anni, il CRISPR, strumento per l'editing genetico (=modifica, rielaborazione di geni), ha trasformato la biologia e ha aperto nuove strade di speranza per correggere malattie mortali ereditarie. Ora, sono iniziati i primi studi clinici (= sull'uomo) con il CRISPR, sperando di curare le malattie prendendo le cellule danneggiate dal paziente, riparandole o sostituendole.
Ma insieme a questa promettente medicina rigenerativa e personalizzata, il CRISPR può avere anche notevoli limitazioni nella sicurezza: può fare modifiche non nel posto giusto (i cosiddetti effetti genetici fuori-bersaglio) o può non essere così efficiente (l'editing può riuscire solo per il 10% dei bersagli disponibili delle cellule).
Queste limitazioni hanno frustrato scienziati come David Brafman dell'Arizona State University, un bioingegnere cellulare. Brafman spera di usare inizialmente l'editing genetico per arrivare al cuore delle cause di malattie neurodegenerative come il morbo di Alzheimer (MA).
“Studiamo le malattie neurodegenerative come il MA e usiamo le cellule staminali per studiare mutazioni specifiche o fattori di rischio associati con il MA”, ha detto Brafman, professore di ingegneria biomedica dell'ASU. “Non siamo necessariamente un laboratorio di sviluppo di strumenti di gene-editing, ma siamo incappati in difficoltà a generare linee di cellule staminali con l'approccio tradizionale di editing basato su CRISPR. Per ragioni che sono ancora sconosciute, le cellule staminali sono veramente resistenti a questo tipo di modifica genetica”.
Luce verde significa 'vai'
Ora, Brafman, usando un nuovo aggiornamento della tecnologia di editing basata su CRISPR sviluppata originariamente nel laboratorio di David Liu ad Harvard, ha ampiamente superato gli sforzi precedenti, producendo un editing di singolo-DNA estremamente preciso delle cellule staminali umane con una efficacia fino al 90%. I risultati sono stati pubblicati sulla rivista Stem Cell Reports.
“In precedenza, con il CRISPR era solo una questione di indovinare”, ha detto Brafman. “E quindi se prendevi cellule staminali a caso e l'efficicia era bassa, era probabile arrivare solo al 10% o al 5%, perché non avevi idea se erano state fatte le modifiche: la cellula non lo dice”.
Il laboratorio di Brafman ha sviluppato il nuovo metodo TREE (Transient Reporter for Editing Enrichment, referente transitorio per l'arricchimento dell'editing) che consente l'arricchimento in massa di popolazioni cellulari editate della base DNA, e per la prima volta, con alta efficacia in linee di cellule staminali umane.
“La maggior parte degli studi sono fatti su linee cellulari immortali o linee cellulari tumorali, che sono relativamente facili da modificare”, ha detto Brafman. “Questo è il primo esempio di uso di editori di base nelle cellule staminali pluripotenti, che è una popolazione di cellule molto importante da modificare geneticamente. Immaginiamo che questo metodo avrà importanti implicazioni per l'uso di linee di cellule staminali umane nella biologia dello sviluppo, nei modelli di malattia, nello screening di farmaci e nelle applicazioni di ingegneria dei tessuti”.
L'anno scorso, questi ricercatori avevano dimostrato che il loro approccio TREE può funzionare sulle linee cellulari umane, ma hanno voluto spingere ulteriormente la tecnologia per trovare un modo per modificare rapidamente ed efficacemente linee di cellule staminali umane.
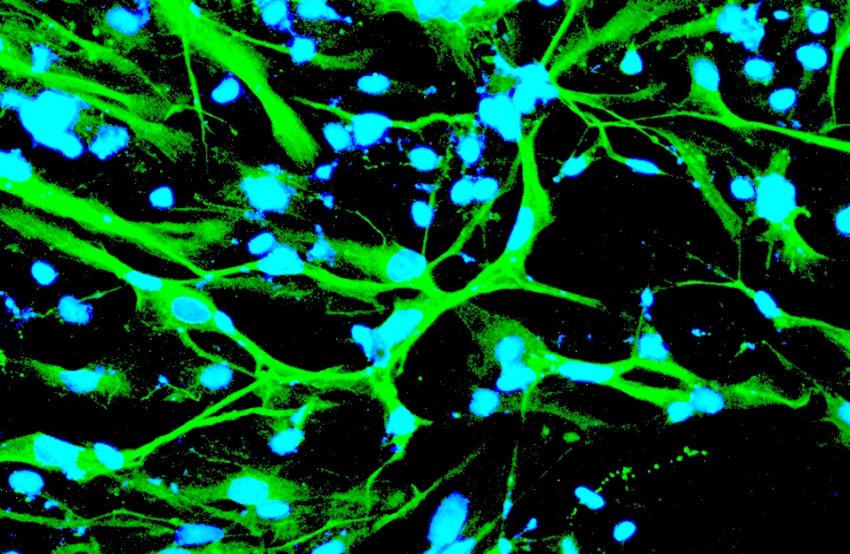
A differenza del CRISPR, che taglia entrambi i filamenti del DNA, il TREE pizzica solo un singolo filamento del DNA. Ad esempio, quando una singola base di DNA viene modificata con successo da un C ad una T, una proteina emette un segnale, virando dal blu al verde.
“Ora, se una cellula si sta dicendo «Se divento verde ho un 90% di possibilità di essere modificata» avrai più fortuna ad identificare le popolazioni modificate“, ha detto Brafman. “Quindi è possibile escludere tutte le cellule che non vengono modificate. Noi isoliamo le cellule singole che stanno brillando di verde, poi le facciamo crescere in una popolazioni clonale che si può far espandere indefinitamente“.
Puntare l'Alzheimer
Le cellule staminali pluripotenti sono prese in considerazione per la medicina rigenerativa, perché hanno la capacità di diventare o di differenziarsi in qualsiasi tipo di cellula del corpo umano.
Brafman spiega che ci sono due fonti generali: “Le cellule staminali embrionali, che derivano dalla massa cellulare interna di blastocisti preimpianto, e poi ci sono le cellule staminali pluripotenti indotte, che derivano dalle cellule somatiche, come la pelle o il sangue, dei pazienti”.
Per la sua ricerca, il laboratorio di Brafman usa le cellule staminali pluripotenti indotte: “Per questo studio, abbiamo usato cellule staminali pluripotenti sia da pazienti sani che da pazienti con MA. Alcuni dei geni che eravamo interessati a modulare sono legati al MA. La maggior parte dei pazienti con MA soffre della forma ad insorgenza tardiva (MA sporadico)“.
Per fornire la loro prova-di-concetto, hanno puntato il gene APOE, che può essere in tre varianti. Una delle tre varianti del gene, chiamato APOE4, è associato ad un rischio più alto del MA ad esordio tardivo. Per lo studio, hanno introdotto modifiche singole basate sul DNA nel gene APOE.
“Ecco perché siamo interessati ad avere queste cellule”, ha detto Brafman. “Rappresentano neuroni e vari tipi di cellule del sistema nervoso centrale nei pazienti con questi fattori di rischio diversi. Quindi siamo in grado di capire perché una variante APOE può aumentare o diminuire il rischio, e poi possiamo iniziare a puntare quei percorsi che sono interessati".
Non solo il TREE è riuscito ad apportare modifiche singole del DNA al gene APOE4, ma a differenza del CRISPR, è riuscito a fare correzioni molto accurate su entrambe le copie del gene APOE4 possedute dagli esseri umani.
“L'approccio tradizionale CRISPR è che devi modificare una volta per ottenere una modifica eterozigota, quindi isolare quel clone, editare di nuovo per ottenere un'altra modifica eterozigota”, ha detto Brafman. “Quindi, quel metodo è molto inefficiente. Stiamo generando modifiche omozigote con un'efficacia vicina al 90%. Non ho visto alcuna altra tecnologia in grado di fare ciò nelle cellule staminali pluripotenti”.
Inoltre, TREE potrebbe anche essere usato per progettare mutazioni cruciali di rimozione (knockout) genetica in linee di cellule staminali.
“L'esperimento più importante che puoi fare se un gene ha implicazioni importanti nelle malattie, nello sviluppo o nella fisiologia, è la sua rimozione”, ha detto Brafman. "Questo apre tutta una serie di questioni che siamo in grado di affrontare. Usando l'APOE come caso di studio, ora siamo in grado di rimuovere l'APOE da queste cellule: non avere del tutto l'APOE è utile, negativo, o senza differenza?”.
Casi complessi
Mentre le malattie come l'anemia falciforme o la fibrosi cistica sono causate da singole mutazioni nel DNA, la maggior parte delle malattie e delle principali cause di morte, come le malattie cardiache o l'ipertensione, sono complesse, coinvolgendo più geni. Brafman voleva anche affrontare la radice delle cause del MA.
“Specialmente per quanto riguarda il MA, ci possono essere molteplici fattori di rischio che agiscono di concerto, quindi volevamo un modo per introdurre più modifiche contemporaneamente nelle cellule staminali pluripotenti. Perché altrimenti, si dovrebbe prendere un approccio iterativo sequenziale, in cui introduci una modifica, isoli una popolazione clonale, introduci un'altra modifica, e così via", ha detto.
I ricercatori sono riusciti a dimostrare che BIG-TREE potrebbe essere usato per produrre nuove linee di cellule staminali modificate contemporaneamente in più posizioni genetiche. I loro risultati hanno mostrato che oltre l'80% dei cloni staminali era stato preso di mira in tutti e tre i diversi siti di geni, e tutti i cloni avevano editato entrambe le copie del gene.
“Abbiamo scoperto che se realizzi più interventi contemporanei ottieni comunque la stessa efficacia di editing come quando modifichi solo un singolo allele”, ha detto Brafman. “Ora, siamo in grado di usare queste cellule come modelli in vitro per studiare la malattia e selezionare farmaci”.
Brafman spera che i nuovi strumenti generino entusiasmo nella comunità di editing genetico, e stimolino gli altri a fare nuove scoperte. “Vogliamo continuare a capire sempre di più quella cassetta degli attrezzi”, ha detto Brafman. “Abbiamo già avuto un alto livello di interesse da altri scienziati che useranno questo metodo per generare le proprie linee di cellule. È una buona cosa".
Fonte: Arizona State University (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Nicholas Brookhouser, Stefan J. Tekel, Kylie Standage-Beier, Toan Nguyen, Grace Schwarz, Xiao Wang, David A. Brafman. BIG-TREE: Base-Edited Isogenic hPSC Line Generation Using a Transient Reporter for Editing Enrichment. Stem Cell Reports, 2020, DOI
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.


 Associazione Alzheimer OdV
Associazione Alzheimer OdV