Il peptide blocca un enzima cerebrale iperattivo che contribuisce alla neurodegenerazione dell'Alzheimer e di altre malattie.
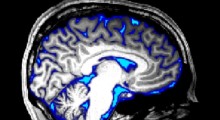
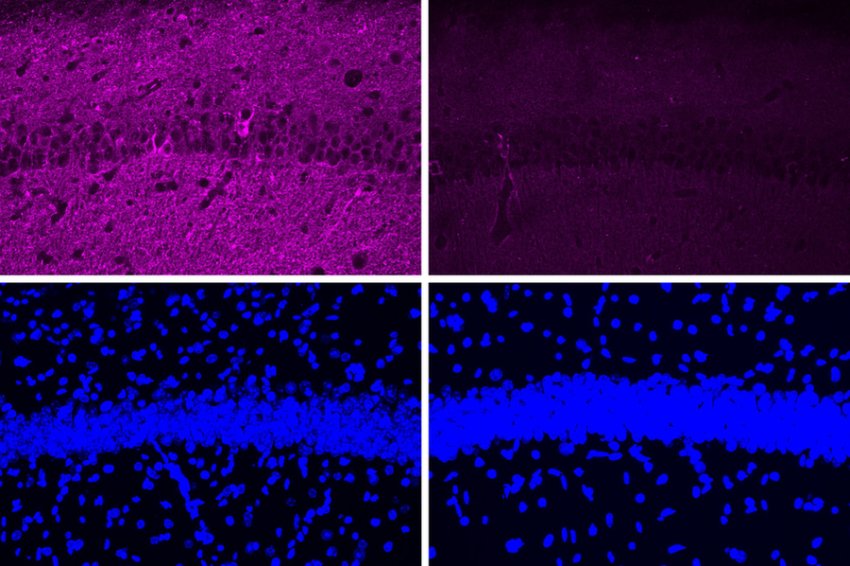 Nel cervello dei topi trattati con il nuovo peptide (due pannelli a destra), si vedono molte meno proteine tau (viola, alto a destra). I pannelli di sinistra mostrano neuroni di topi trattati con una versione alterata del peptide. Nei due pannelli inferiori, in blu il DNA nei nuclei cellulari che dimostra che i cambiamenti nei livelli di tau non sono causati da cambiamenti significativi nella popolazione cellulare. (Fonte: Ping-Chieh Pao/MIT)
Nel cervello dei topi trattati con il nuovo peptide (due pannelli a destra), si vedono molte meno proteine tau (viola, alto a destra). I pannelli di sinistra mostrano neuroni di topi trattati con una versione alterata del peptide. Nei due pannelli inferiori, in blu il DNA nei nuclei cellulari che dimostra che i cambiamenti nei livelli di tau non sono causati da cambiamenti significativi nella popolazione cellulare. (Fonte: Ping-Chieh Pao/MIT)
Neuroscienziati del MIT di Boston hanno trovato un modo per invertire la neurodegenerazione e altri sintomi del morbo di Alzheimer (MA) interferendo con un enzima che di solito è iperattivo nel cervello dei pazienti, con uno studio appena apparso su PNAS.
Quando i ricercatori hanno trattato dei topi con un peptide che blocca la versione iperattiva dell'enzima chiamato CDK5, hanno trovato una drastica riduzione della neurodegenerazione e del danno al DNA nel cervello. Questi topi hanno anche mostrato miglioramenti nella capacità di svolgere compiti come apprendere a navigare in un labirinto d'acqua.
"Abbiamo scoperto che l'effetto di questo peptide è semplicemente notevole", afferma Li-Huei Tsai, direttrice del Picower Institute for Learning and Memory del MIT e autrice senior dello studio. "Abbiamo visto effetti meravigliosi in termini di riduzione della neurodegenerazione e delle risposte neuroinfiammatorie e persino dei deficit comportamentali".
Con ulteriori test, i ricercatori sperano che il peptide possa infine essere usato come trattamento dei pazienti con MA e altre forme di demenza che hanno sovra-eccitazione del CDK5. Il peptide non interferisce con il CDK1, un enzima essenziale che è strutturalmente simile al CDK5, ed è simile per dimensione ad altri farmaci peptidici usati nelle applicazioni cliniche.
Puntare il CDK5
La Tsai ha studiato il ruolo del CDK5 nel MA e in altre malattie neurodegenerative fin dall'inizio della sua carriera. Come postdottorato, ha identificato e clonato il gene CDK5, che codifica un tipo di enzima noto come 'chinasi ciclina-dipendente' (CDK, cyclin-dependent kinase). La maggior parte degli altri chinasi dipendenti dalla ciclina è coinvolto nel controllo della divisione cellulare, ma il CDK5 non lo è. Al contrario, ha ruoli importanti nello sviluppo del sistema nervoso centrale e aiuta anche a regolare la funzione sinaptica.
Il CDK5 è attivato da una proteina più piccola con cui interagisce, chiamata P35. Quando la P35 si lega al CDK5, la struttura dell'enzima cambia, consentendogli di fosforilare i suoi bersagli (aggiunge una molecola di fosfato). Tuttavia, nel MA e in altre malattie neurodegenerative, la P35 è divisa in una proteina più piccola chiamata P25, che può anche legarsi al CDK5 ma ha un'emivita più lunga rispetto alla P35.
Se si lega alla P25, il CDK5 diventa più attivo nelle cellule. La P25 consente inoltre al CDK5 di fosforilare molecole diverse dai suoi soliti obiettivi, compresa la proteina tau. Le proteine tau iperfosforilate formano i grovigli neurofibrillari che sono una delle caratteristiche del MA.
Nei lavori precedenti, il laboratorio della Tsai ha dimostrato che i topi transgenici progettati per esprimere P25 sviluppano una neurodegenerazione grave. Nell'uomo, la P25 è stata collegata a diverse malattie, non solo al MA, ma anche al Parkinson e alla demenza frontotemporale.
Le aziende farmaceutiche hanno cercato di puntare la P25 con farmaci a piccole molecole, ma questi farmaci tendono a causare effetti collaterali perché interferiscono anche con altre chinasi ciclina-dipendenti, quindi nessuno di essi è stato testato nei pazienti.
Il team del MIT ha deciso di adottare un approccio diverso per puntare la P25, usando un peptide anziché una piccola molecola. Hanno progettato il loro peptide con una sequenza identica a quella di un segmento di CDK5 noto come 'loop T', che è una struttura critica per legare il CDK5 alla P25. L'intero peptide è lungo solo 12 aminoacidi, leggermente più lungo della maggior parte dei farmaci peptidici esistenti, che sono lunghi da 5 a 10 aminoacidi.
"Dal punto di vista del farmaco peptidico, di solito piccolo è meglio", afferma la Tsai. "Il nostro peptide è quasi all'interno di quella dimensione molecolare ideale".
Effetti drastici
Nei test su neuroni coltivati in piatto in laboratorio, i ricercatori hanno scoperto che il trattamento con il peptide ha portato a una moderata riduzione dell'attività del CDK5. Tali test hanno anche mostrato che il peptide non inibisce il normale complesso CDK5-P35, né influisce su altri chinasi ciclina-dipendenti.
Quando i ricercatori hanno testato il peptide in topi modello del MA con CDK5 iperattivo, hanno visto una miriade di effetti benefici, tra cui la riduzione del danno al DNA, dell'infiammazione neurale e della perdita di neuroni. Questi effetti sono stati molto più pronunciati nei topi che nelle cellule in coltura.
Il trattamento peptidico ha anche prodotto drastici miglioramenti in topi di modello diverso di Alzheimer, che hanno una forma mutante della proteina tau che porta a grovigli neurofibrillari. Dopo il trattamento, quei topi hanno mostrato riduzioni sia nelle patologie tau che nella perdita di neuroni.
Insieme a quegli effetti nel cervello, i ricercatori hanno anche osservato miglioramenti comportamentali. I topi trattati con il peptide sono andati molto meglio in un'attività che richiede di apprendere come navigare in un labirinto d'acqua, basata sulla memoria spaziale, rispetto ai topi che erano stati trattati con un peptide di controllo (una versione alterata del peptide usato per inibire il CDK5-P25).
In quegli studi sui topi, i ricercatori hanno iniettato il peptide e hanno scoperto che era in grado di attraversare la barriera emato-encefalica e raggiungere i neuroni dell'ippocampo e di altre parti del cervello. I ricercatori hanno anche analizzato i cambiamenti nell'espressione genica che si verificano nei neuroni di topo dopo il trattamento con il peptide.
Tra i cambiamenti che hanno osservato c'era un aumento dell'espressione di circa 20 geni che sono in genere attivati da una famiglia di regolatori genici chiamati MEF2. Il laboratorio della Tsai aveva dimostrato in precedenza che l'attivazione di MEF2 di questi geni può conferire resilienza alla compromissione cognitiva nel cervello delle persone con grovigli tau, e lei ipotizza che il trattamento peptidico possa avere effetti simili.
"Uno sviluppo ulteriore di tali inibitori peptidici verso un candidato terapeutico primario, se dimostra di essere selettivo per il bersaglio e relativamente privo di effetti collaterali clinici, può infine portare a nuovi trattamenti per i disturbi neurodegenerativi che vanno dal MA alla demenza frontotemporale, al Parkinson", dice Stuart Lipton, professore di neuroscienze dello Scripps Research, non coinvolto nello studio.
La Tsai ora prevede di fare ulteriori studi su altri topi modello di malattie che coinvolgono la neurodegenerazione associata alla P25, come la demenza frontotemporale, la demenza indotta da HIV e la compromissione cognitiva legata al diabete.
"È molto difficile dire con precisione quale malattia trarrà i maggiori benefici, quindi penso che sia necessario molto più lavoro", afferma.
Fonte: Anne Trafton in Massachusetts Institute of Technology (> English) - Traduzione di Franco Pellizzari.
Riferimenti: Ping-Chieh Pao, ...[+16], Li-Huei Tsai. A Cdk5-derived peptide inhibits Cdk5/p25 activity and improves neurodegenerative phenotypes. PNAS, 12 Apr 2023, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.






 Associazione Alzheimer OdV
Associazione Alzheimer OdV